 |
애경산업이 국내로 들여온 2080 치약 수입 제품 상당수에서 사용 금지 성분인 트리클로산이 검출됐다. 국내 치약 시장을 대표하며 '국민 치약'으로 자리 잡아온 애경산업의 2080 치약 브랜드 신뢰도에 적잖은 타격이 불가피해졌다. 식품의약품안전처(식약처)는 문제 제품 회수와 함께 애경산업에 대한 행정처분 절차에 착수했다.
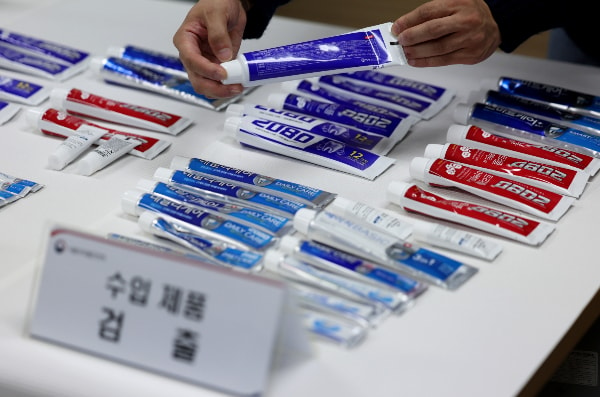
식품의약품안전처는 지난 20일 오후 서울 양천구 서울지방식약청에서 진행한 브리핑에서 애경산업의 2080 수입 치약 전 제조번호 제품 및 국내 제조 치약에 대한 트리클로산 검사 결과를 발표했다.
검사 결과 애경산업이 해외 제조소 도미(Domy)에서 들여온 2080 치약 수입 제품(6종) 870개 제조번호 중 754개 제조번호에서 트리클로산이 최대 0.16% 검출됐다. 시중에 유통된 물량은 약 2900만개로, 회수는 다음 달 4일 완료될 예정이다. 애경산업이 국내에서 제조한 128종에서는 트리클로산이 모두 검출되지 않았다.
트리클로산은 제품 변질을 막기 위한 보존제로 사용돼 왔지만, 국내에서는 2016년부터 구강용품에 사용이 금지됐다. 식약처 조사 결과 수입 치약 제품에 트리클로산이 검출된 것은 도미가 2023년 4월부터 치약 제조 장비의 소독을 위해 트리클로산을 사용해 온 데 따른 것으로 조사됐다. 이에 따라 제조 장비에 잔류한 트리클로산 성분이 치약 제품에 섞였고, 작업자별 소독 방식과 사용량 차이로 인해 제품별 잔류량이 일관하지 않게 나타났다.
애경산업에 대해 현장점검을 실시한 결과 ▲회수에 필요한 조치가 지연되는 등 회수 절차를 준수하지 않은 점 ▲해외 제조소에 대한 수입 품질관리가 미비한 점 ▲트리클로산이 섞인 수입 치약을 국내에 유통한 점 등이 확인됐다. 이에 따라 식약처는 애경산업에 대한 행정 처분 절차 등을 진행할 방침이다.
다만 식약처는 위해 평가 전문가 자문 결과 트리클로산이 0.3% 이하로 함유된 치약 사용에 따른 위해 발생 우려는 낮은 수준이라고 설명했다. 유럽 등 일부 국가에서도 치약에 트리클로산이 0.3% 이하로 쓰일 경우 안전하다고 평가한다.
식약처는 국민 불안을 고려해 수입 치약 관리 체계를 전면 강화하기로 했다. 앞으로 수입자가 치약을 최초 수입할 때 트리클로산 성적서를 제출하도록 하고, 판매 시에는 제조번호별 트리클로산 자가품질검사를 의무화한다. 유통 단계에서 식약처가 매년 모든 수입 치약에 대해 트리클로산 함유 여부를 전수조사하는 등 수거·검사를 확대한다.
수입 치약의 해외 제조소 점검 대상을 확대해 트리클로산 등 국내 금지된 성분의 혼입 여부 등도 집중적으로 점검한다. 아울러 치약을 포함한 모든 의약외품의 위해 우려 성분 모니터링 주기를 5년에서 3년으로 단축한다. 이와 함께 치약에 대한 의약외품 제조·품질관리기준(GMP) 단계적 의무화 검토와 함께 유해한 의약외품 제조·수입으로 취득한 경제적 이익 환수를 위한 징벌적 과징금 부과의 법적 근거 마련도 추진한다.
식약처는 "치약의 안전성에 대해 꼼꼼히 살피고 국민이 안심할 수 있도록 치약 등 의약외품 안전관리를 강화하겠다"고 전했다.